栏目: 学习方法 学科核心素养 作者:佚名 热度:
化学给人以知识,化学史给人以智慧。
每一个高中生不仅要学好化学知识,更要能依据化学方法探究未知世界,这也是化学核心素养的体现,高中有五大化学核心素养,接下来为大家一一讲解。
素养一:宏观辨识与微观探析
能通过观察、辨析一定条件下物质的形态及变化的宏观现象,初步掌握物质及其变化的分类方法,并能运用符合表征物质及其变化;能从物质的微观层面理解其组成、结构和性质的联系,形成“结构决定性质,性质决定应用”的观念;能根据物质的微观结构预测物质在特定条件下可能具有的性质和可能发生的变化。
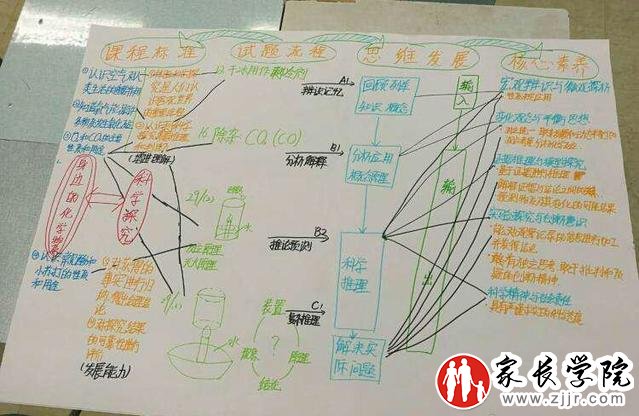
例一:石墨炔碳纳米结心材料,由于其特殊的电子结构及优异的性能,有望得以广泛应用。石墨炔的结构片断如图所示,下列叙述正确的是()
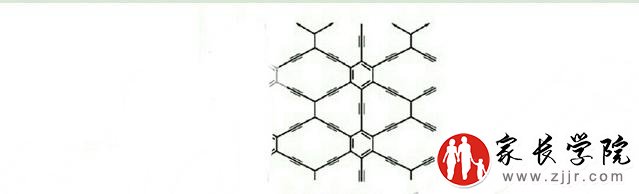
A.石墨炔属于烃类B.有3种不同的碳碳键C.是电的良导体D.所有碳原子共平面
命题意图:试题考查考生的观察理解能力、联想迁移能力,力图体现核心养中“结构决定性质,性质决定应用”的观念
解析:由结构图知,每一个碳原子以4个键与其他碳原子相连,石墨炔中有H原子,所以石墨炔不属于烃,是碳的一种新的单质,A错;结构图中,有碳单键、碳碳双键、碳碳三键和苯环中的独特的碳碳键,共有4种不同的碳碳,B错;碳原子最外层的4个价电子均形成共价键,没有自由移动的电子,所石墨炔不是电的良导体,C错;联想乙烯(键角约为120)、乙炔(键角约为180)的结构可知,石墨炔分子中的所有碳原子共平面,D正确。

素养二:变化观念与平衡思想
能认识物质是在不断运动的,物质的变化是有条件的:能从内因和外因、量变与质变等方面较全面地分析物质的化学变化,关注化学变化中的能量转化从不同视角对纷繁复杂的化学变化进行分类研究,逐步揭示各类变化的特征和律;能用对立统一、联系发展和动态平衡的观点考察、分析化学反应,预测在条件某种物质可能发生的化学变化
例二:

命题意图:柔性电子技术有可能带来一场电子技术革命。目前柔性储能器件相对较低的理论能量密度限制其在柔性电子产品中的进一步应用,该研究成果为具有超高能量密度的锂空气电池应用于柔性电子器件提供了可能性。该题力图体现“能对与化学有关的社会热点问题做出正确的价值判断”的核心素养要求。
解析:纤维素不导电,石墨导电,故放电时,纸张表面毛笔书写后留下的石墨为电池正极,A错;原电池或电解池工作时,电解质中阴、阳离子的移动方向一般遵循“阴阳相吸”,即电池放电时,电解质中的阳离子移向阴极(电池的正也可以叫阴极),据此可快速判断放电时,带正电荷的Li由负极经过有机电解质溶液移向正极(阴极),B错;充电时,直流电源负极与电池负极(金属锂)相连故x为负极,C错;充电时,空气电极作阳极,此时LiO2失去电子生成O2:Li2O-2e=O2+2Li,D正确
素养三:证据推理与模型认知
能初步学会收集各种证据,对物质的性质及其变化提出可能的假设:基于证进行分析推理,证实或证伪假设:能解释证据与结论之间的关系,确定形成科结论所需要的证据和寻找证据的途径:能认识化学现象与模型之间的联系,能用多种模型来描述和解释化学现象,预测物质及其变化的可能结果;能依据物及其变化的信息建构模型,建立解决复杂化学问题的思维框架。
例三:


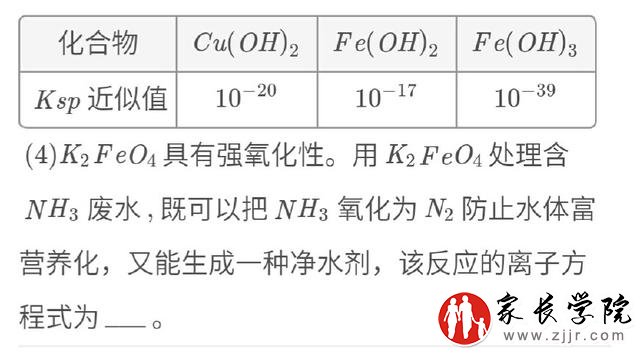
题意图生根据实验探究过程发现的实验现象,通过对、演绎、归纳等手段,产生新的问题,走向深度学习:或依据探究目的优化实方案或改进实验的设想,走向深度学习;或尊重事实和证据,不迷信权威,在疑和批判中提出问题,走向深度学习等等。解析:(1)根据化学反应原理,发生的反应为CaO2+2HCl=CaCl2+2O2、2H2O2=2H2O+O2,总反应程式为2CaO2+4HCl=2CaCl2+2H2O2。
溶液a中存在较多的H2O2,双氧水具有强氧化性,能使石蕊溶液褪色2)首先应制取氧气,再干燥,然后与钙反应,还应防止空气中的水蒸气进硬质玻璃管干扰反应,故连接顺序为dcfbce 反应结束后,熄灭酒精灯,待反应管冷却至室温,关闭分液漏斗的活塞。(3)NH3和反应生成的H,使溶液显碱性,减少CaO28H2O的溶解,提高产品的产率过滤需要的玻璃仪器为烧杯、漏斗、玻璃棒。洗涤沉淀的操作为:沿玻璃棒向斗中注入蒸馏水至浸没沉淀,让水自然流下,重复2至3次。(4)在FeCl2溶液中加KSCN溶液,溶液不显红色,再加入少量CaO2粉末,溶液变红色,说明CaO氧化性比FeCl3的氧化性强答案:(1)2CaO2 +4HCl=2CaCl2 +2H2O +O2 H2O(2)defbce(或defcbe)
熄灭酒精灯,待反应管冷却至室温,关闭分液漏斗的活塞3)中和生成的氢离子促进反应进行(或使溶液呈碱性,减少CaO28H2O解,或提高产品的产率等其他合理答案)
烧杯、漏斗、玻璃棒沿玻璃棒向漏斗中注入蒸馏水至浸没沉淀,让水自然流下,重复2至3次在FeCl2溶液中滴加KSCN溶液,溶液不呈红色,再加入少量CaO2粉末液变红色,说明CaO2的氧化性比FeCl3的氧化性强


素养四:实验探究与创新意识
发现和提出有探究价值的化学问题,能依据探究目的设计并优化实验方案,完成实验操作,能对观察记录的实验信息进行加工并获得结论;提出进一步探究或改进实验的设想、和同学交流实验探究获得的成果;能尊重事实和证据,不迷信权威,具有独立思考、敢于质疑和批判的创新精神。

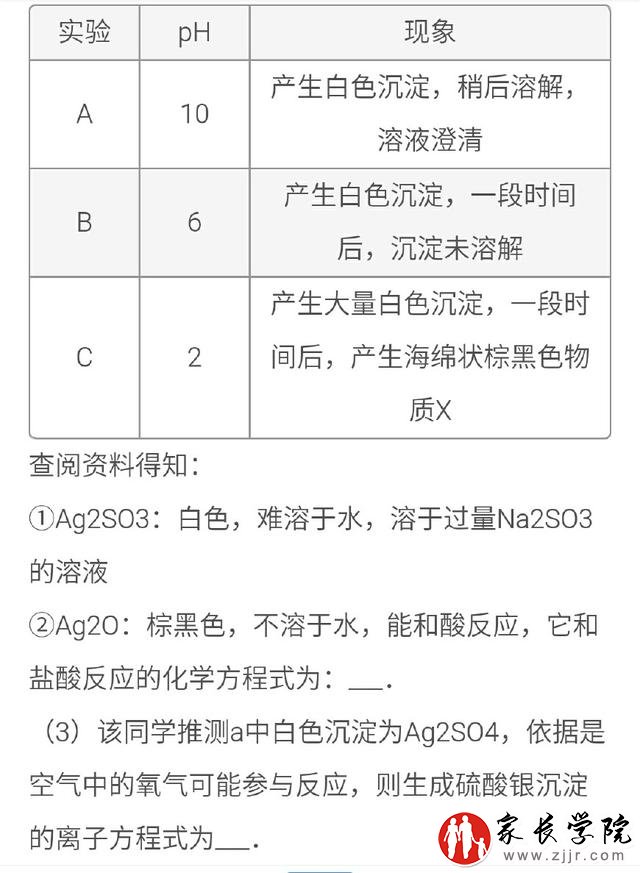


命题意图:考察学生“能初步学会收集各种证据,对物质的性质及可能发生的变化提出假设;能解释证据和结论之间的联系,确定形成科学结论所需要的证据和寻找证据的正确途径”。

解析:(1)因SO3水解产生OH,故Na2SO3溶液显碱性;因Ag水解产生氢离子,故AgNO3溶液显酸性。(2)氧气参与反应生成硫酸银沉淀的离子方程式为2Ag+2SO3=Ag2SO4;结合已知信息知Ag2SO3难溶于水,溶于过量的Na2SO3液,故可知沉淀为Ag2SO3,由于b、c中的沉淀能溶于Na2SO3溶液,而Ag2SO4固体不溶于Na2SO3(4)加稀盐酸无明显现象说明X中不含有Ag2O;用Ba(NO3)2溶液、BaCl2液检验二中反应后的溶液,前者无变化,后者产生白色沉淀,可知溶液里没有硫酸根离子,有Ag,则X为Ag;Ag被浓硝酸氧化为AgNO3,同时生成了红棕色的O2:Ag+2HNO3(浓)=AgNO3+NO2+ H2O(5)通入Y气体是为了增加溶液的酸性,同时不影响溶液里 4价硫的还原,故选择二氧化硫气体比较适宜。答案:(1)SO3、Ag(2)Ag20+2HCI=2AgCI+H2O(3)2Ag+2SO3+O2= Ag2SO4+SO4 Na2SO3, (4)证明X不是氧化银;Ag;Ag+2HNO3(浓)=AgNO3+NO2+ H2O(5) 二氧化硫;Ag2SO3+H2O=2Ag+H2SO4(由于作者水平有限,离子符合无法打出,导致部分内容较抽象,请同学们谅解)

素养五:科学精神与社会责任
具有终身学习的意识和严谨求实的科学态度;崇尚真理,形成真理面前人人平等的意识:关注与化学有关的社会热点问题,认识环境保护和资源合理开发的重要性,具有可持续发展意识和绿色化学观念;深刻理解化学、技术、社会和环境之间的相互关系,赞赏化学对社会发展的重大贡献,能运用已有知识和方法综合分析化学过程对自然可能带来的各种影响,权衡利弊,勇于承担责任,积极参与有关化学问题的社会决策。
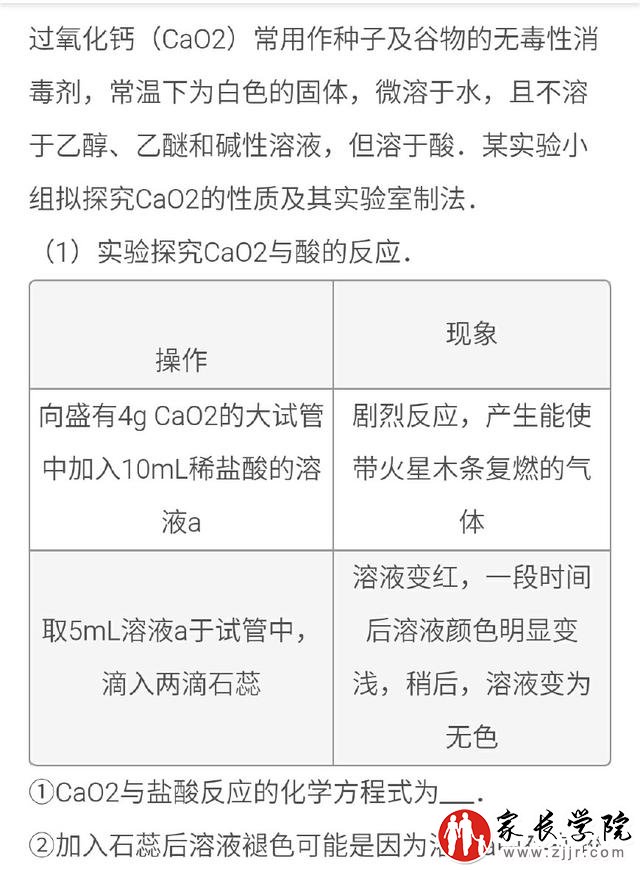
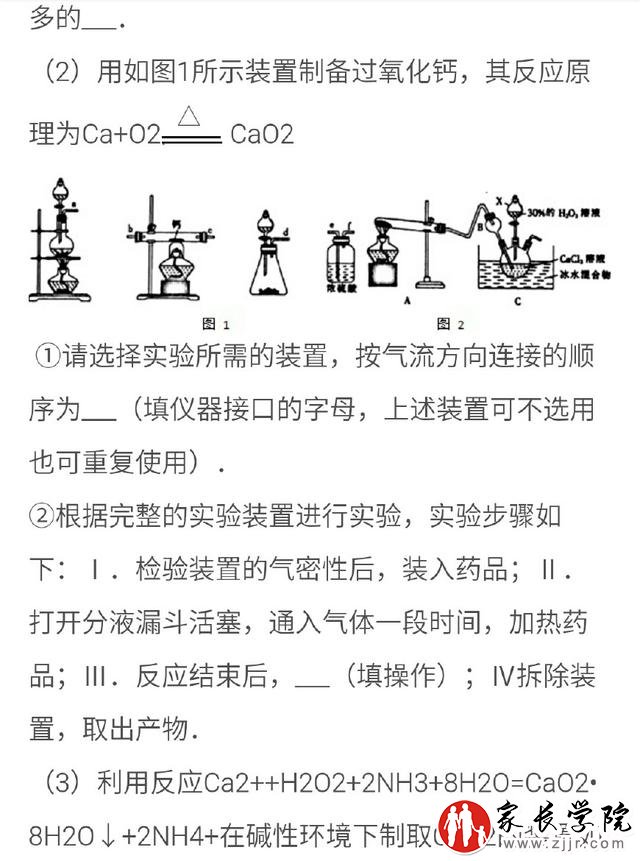

命题意图:试题力图考查学生根据实验探究过程发现的实验现象,通过演绎、归纳等手段,产生新的问题,走向深度学习;或依据探究目的优化实方案或改进实验的设想,走向深度学习;或尊重事实和证据,不迷信权威,在疑和批判中提出问题,走向深度学习等等
解析:(1)根据化学反应原理,发生的反应为CaO2+2HCl=CaCl2+2O2、2H2O2=2H2O+O2,总反应方式为2CaO2+4HCl=2CaCl2+2H2O+O2;溶液a中存在较多的H2O2,双氧具有强氧化性,能使石蕊溶液褪色2)首先应制取氧气,再干燥,然后与钙反应,还应防止空气中的水蒸气进入硬质玻璃管干扰反应,故连接顺序为defcba;反应结束后,熄灭酒精灯,待反应管冷却至室温,关闭分液漏斗的活塞。(3)NH和反应生成的H,使溶液显碱性,减少CaO28H2O的溶解,提高产品的产率;过滤需要的玻璃仪器为烧杯、漏斗、玻璃棒。洗涤沉淀的操作为:沿玻璃棒向斗中注入蒸馏水至浸没沉淀,让水自然下,重复2至3次。(4)在FeCl2溶液中滴加KSCN溶液,溶液不显红色,再加入少量CaO2粉末,溶液变红色,说明CaO的氧化性比FeCl3的氧化性强答案:(1)2CaO2+4HCl=2CaCl2+2H2O+O2;H2O(2)defbce或defcbe2熄灭酒精灯,待反应管冷却至室温,关闭分液漏斗的活塞(3)中和生成的氢离子,促进反应进行(使溶液呈碱性,减少CaO28H2O的溶解,或提高产品的产率等其他合理答案;烧杯、漏斗、玻璃棒沿玻璃棒向漏斗中注入蒸馏水至浸没沉淀,让水自流下,重复2至3次(4)在FeCl2溶液中滴加KSCN溶液,溶液不呈红色,再加入少量CaO2粉末液变红色,说明CaO2的氧化性比FeCl3的氧化性强

版权声明:文章观点仅代表作者观点,作为参考,不代表本站观点。部分文章来源于网络,如果网站中图片和文字侵犯了您的版权,请联系我们及时删除处理!转载本站内容,请注明转载网址、作者和出处,避免无谓的侵权纠纷。
上一篇:思想政治学科核心素养的基本内涵
下一篇:物理学科核心素养
相关推荐